Каталитическое окисление: механизмы, кинетика и особенности процесса
Рассмотрен механизм каталитического окисления ЛОС на макроуровне (в реакторе) и молекулярном уровне
Катализом называют процесс изменения скорости протекания химических реакций в присутствии катализаторов. Катализатор — это химическое соединение, которое многократно вступает в промежуточные взаимодействия и полностью восстанавливает свой состав после каждого цикла реакций.
Действие катализаторов принципиально отличается от действия таких факторов, как температура или давление. Основное отличие состоит в том, что катализатор не влияет на равновесие химической реакции. Изменяя в равной степени скорость прямой и обратной реакций, он лишь способствует более быстрому достижению равновесия при данных условиях. В отличие от температуры, катализаторы не влияют на скорость диффузии. Поэтому во многих случаях при значительном повышении скорости химической реакции суммарная скорость процесса остается низкой из-за медленного подвода компонентов в зону реакции.
Действие катализаторов принципиально отличается от действия таких факторов, как температура или давление. Основное отличие состоит в том, что катализатор не влияет на равновесие химической реакции. Изменяя в равной степени скорость прямой и обратной реакций, он лишь способствует более быстрому достижению равновесия при данных условиях. В отличие от температуры, катализаторы не влияют на скорость диффузии. Поэтому во многих случаях при значительном повышении скорости химической реакции суммарная скорость процесса остается низкой из-за медленного подвода компонентов в зону реакции.
Термодинамические и кинетические аспекты катализа
Скорость процесса U выражают изменением количества продукта Gп, его концентрации Cп и степени превращения основного исходного вещества в единицу времени. Для процессов в проточных реакторах, выражение скорости процесса будет иметь вид:
где, v – реакционный объем (в гетерогенно-каталитических процессах – насыпной объем катализатора); k – константа скорости процесса; ΔC- движущая сила процесса (произведение действующих концентраций реагирующих веществ).
Скорость реакции можно увеличить, повышая концентрации реагентов С и давление P до оптимальных значений. Перемешивание приводит к увеличению k только в случаях медленной диффузии реагентов в зону реактора. Температура является наиболее универсальным средством интенсификации технологических процессов, повышение ее ускоряет химические реакции и диффузию. Однако рост температуры ограничен термостойкостью материалов и в обратимых экзотермических процессах приводит к уменьшению ΔC. Таким образом, ускоряющее действие всех параметров технологического режима, за исключением действия катализаторов, возможно лишь до определенного предела.
Суть каталитического действия заключается в изменении пути реакции. Химическое превращение протекает через образование активного комплекса, обладающего избыточной энергией. Если необходимая энергия активации E1 велика, реакция практически не протекает. Катализатор открывает новый путь: он вступает в промежуточное химическое взаимодействие, образуя активный комплекс с меньшей энергией активации E2. После второго этапа реакции катализатор восстанавливает свой состав.
Начальное и конечное состояния системы одинаковы как в случае с катализатором, так и без него — катализатор не изменяет равновесие, но увеличивает скорость превращения.
где, v – реакционный объем (в гетерогенно-каталитических процессах – насыпной объем катализатора); k – константа скорости процесса; ΔC- движущая сила процесса (произведение действующих концентраций реагирующих веществ).
Скорость реакции можно увеличить, повышая концентрации реагентов С и давление P до оптимальных значений. Перемешивание приводит к увеличению k только в случаях медленной диффузии реагентов в зону реактора. Температура является наиболее универсальным средством интенсификации технологических процессов, повышение ее ускоряет химические реакции и диффузию. Однако рост температуры ограничен термостойкостью материалов и в обратимых экзотермических процессах приводит к уменьшению ΔC. Таким образом, ускоряющее действие всех параметров технологического режима, за исключением действия катализаторов, возможно лишь до определенного предела.
Суть каталитического действия заключается в изменении пути реакции. Химическое превращение протекает через образование активного комплекса, обладающего избыточной энергией. Если необходимая энергия активации E1 велика, реакция практически не протекает. Катализатор открывает новый путь: он вступает в промежуточное химическое взаимодействие, образуя активный комплекс с меньшей энергией активации E2. После второго этапа реакции катализатор восстанавливает свой состав.
Начальное и конечное состояния системы одинаковы как в случае с катализатором, так и без него — катализатор не изменяет равновесие, но увеличивает скорость превращения.
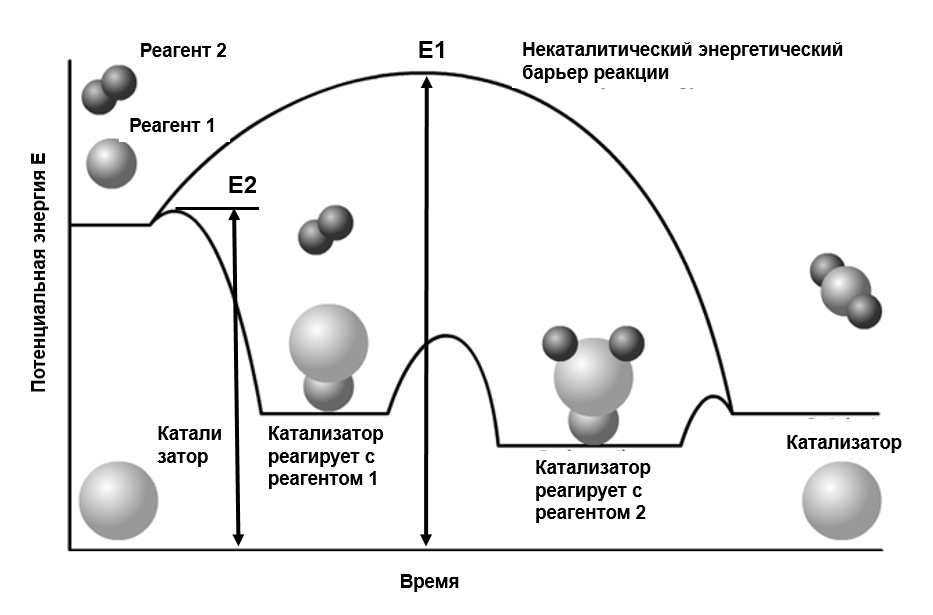
Изменение энергии системы при реакции каталитического окисления
E1 - энергия активации некаталитической реакции
E2 - энергии активации начальной стадий каталитического процесса
E1 - энергия активации некаталитической реакции
E2 - энергии активации начальной стадий каталитического процесса
Классификация и селективность
Каталитические реакции окисления преимущественно относятся к гетерогенным, где катализатор находится в твердой фазе, а реагенты — в газовой.
Катализаторы окисления делятся на два типа:
Катализаторы окисления делятся на два типа:
- Катализаторы неполного (парциального) окисления: Многокомпонентные оксиды V-VIII групп (используются для получения формальдегида из метанола, дегидрирования бутилена).
- Катализаторы глубокого окисления: Металлы платиновой группы (Pt, Pd, Rh), а также сложные оксиды VI-VIII групп.
Стадийность и механизмы окислительного процесса
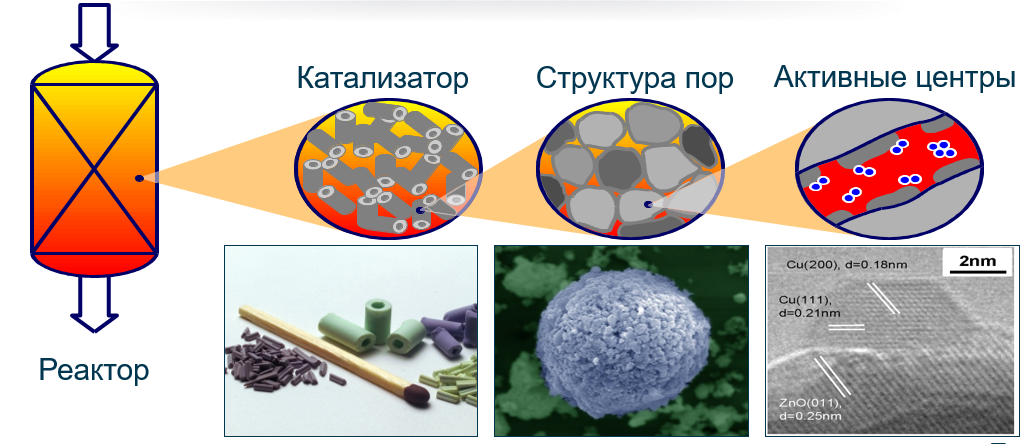
Каталитическое окисление представляет собой совокупность реакций на поверхности твердых пористых катализаторов с процессами подвода и отвода реагентов. Процесс состоит из следующих элементарных стадий:
- Эффективная внешняя диффузия реагентов из основного потока к поверхности зерен катализатора.
- Эффективная внутренняя диффузия в порах зерна.
- Активированная адсорбция (хемосорбция) реагентов с образованием поверхностного химического соединения.
- Перегруппировка атомов с образованием поверхностных комплексов «продукт-катализатор».
- Десорбция продукта и регенерация активного центра.
- Диффузия продуктов в порах зерна.
- Диффузия продукта от поверхности зерна в основной поток газа.
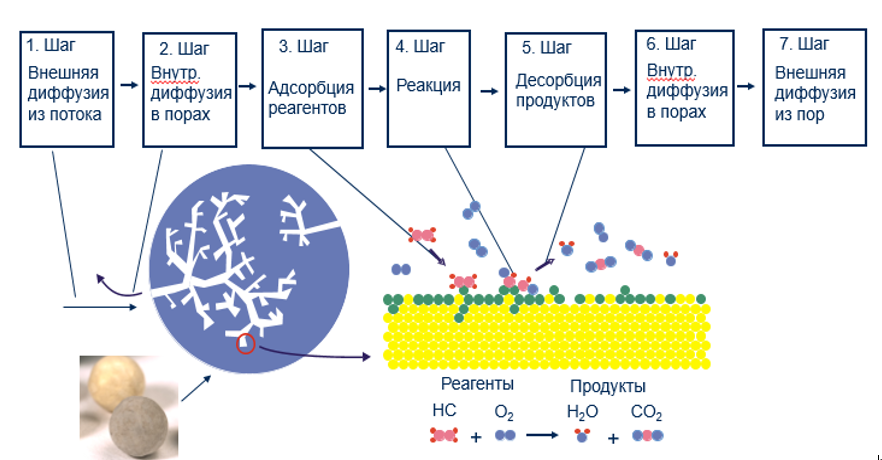
Стадии процесса каталитического окисления:
Схематичное изображение пористого зерна катализатора. Поток газа (1) подходит к внешней поверхности, молекулы реагентов диффундируют внутрь пор (2), адсорбируются на активном центре (3), вступают в реакцию (4), после чего продукты десорбируются (5) и диффундируют обратно в поток (6, 7).
Схематичное изображение пористого зерна катализатора. Поток газа (1) подходит к внешней поверхности, молекулы реагентов диффундируют внутрь пор (2), адсорбируются на активном центре (3), вступают в реакцию (4), после чего продукты десорбируются (5) и диффундируют обратно в поток (6, 7).
Механизмы каталитического ускорения
- Стадийный (окислительно-восстановительный): Предполагает диссоциативную хемосорбцию кислорода с последующим взаимодействием активированного кислорода с органическим веществом.
- Деформационный: Образование общего активированного комплекса из органического вещества и кислорода на катализаторе.
- Гетерогенный: Все стадии протекают на поверхности катализатора без десорбции промежуточных продуктов.
- Гетерогенно-гомогенный (радикально-цепной): Катализатор инициирует зарождение радикалов, которые десорбируются и развивают цепь в газовой фазе. Для целей очистки газов этот механизм нежелателен, так как приводит к образованию токсичных продуктов неполного окисления (CO, альдегиды).
Слитный и раздельный механизмы окисления:
Ключевым вопросом является происхождение кислорода в продуктах реакции.
- Слитный механизм: Кислород адсорбируется на поверхности и взаимодействует с адсорбированной молекулой углеводорода в рамках единого акта. Схема: O2+B+K→OВК→K+BO
- Раздельный (стадийный) механизм: Реакция идет через кислород решетки катализатора. Сначала катализатор окисляется кислородом газовой фазы, затем органическое вещество восстанавливает катализатор, забирая кислород решетки. Схема: O2+K→KO ; KO+B→K+BO
Формы адсорбции и роль поверхностных комплексов
Характер адсорбции определяет путь реакции. При низких температурах преобладает физическая адсорбция, при повышении температуры — хемосорбция. Кислород может адсорбироваться в формах O2,O2−,O−. Органические вещества образуют на поверхности углеводород-кислородные комплексы.
Важной особенностью глубокого окисления является образование продуктов окислительного уплотнения — высокомолекулярных соединений, накапливающихся на поверхности катализатора (до 15–20% от массы). В ряде случаев лимитирующей стадией является не взаимодействие исходного вещества с кислородом, а окисление этих уплотненных структур, которые служат промежуточными предшественниками CO2.
Важной особенностью глубокого окисления является образование продуктов окислительного уплотнения — высокомолекулярных соединений, накапливающихся на поверхности катализатора (до 15–20% от массы). В ряде случаев лимитирующей стадией является не взаимодействие исходного вещества с кислородом, а окисление этих уплотненных структур, которые служат промежуточными предшественниками CO2.
Кинетические области гетерогенного катализа
Интенсивность процесса определяется соотношением скоростей химической реакции имеет высокий температурный коэффициент γ=2–4 и диффузии имеет низкий температурный коэффициент γ=1,1–1,3. В зависимости от температуры и размера зерен различают области протекания процесса:
I. Кинетическая область: Низкие температуры. Скорость химической реакции мала по сравнению с диффузией. Энергия активации высока и постоянна. Скорость зависит от температуры, но не зависит от скорости потока и размера зерен. Наблюдается пропорциональность скорости удельной поверхности катализатора.
II. Внутридиффузионная область: Средние температуры. Химическая реакция ускоряется, но диффузия реагентов вглубь пор не успевает за ней. Энергия активации кажущаяся (снижается в 2 раза). Скорость зависит от пористости и размера зерен, но слабо зависит от линейной скорости потока.
III. Внешнедиффузионная область: Высокие температуры. Реакция идет мгновенно на внешней поверхности. Лимитирует перенос вещества из ядра потока к зерну. Энергия активации близка к нулю. Скорость сильно зависит от гидродинамики (скорости потока) и практически не зависит от температуры.
I. Кинетическая область: Низкие температуры. Скорость химической реакции мала по сравнению с диффузией. Энергия активации высока и постоянна. Скорость зависит от температуры, но не зависит от скорости потока и размера зерен. Наблюдается пропорциональность скорости удельной поверхности катализатора.
II. Внутридиффузионная область: Средние температуры. Химическая реакция ускоряется, но диффузия реагентов вглубь пор не успевает за ней. Энергия активации кажущаяся (снижается в 2 раза). Скорость зависит от пористости и размера зерен, но слабо зависит от линейной скорости потока.
III. Внешнедиффузионная область: Высокие температуры. Реакция идет мгновенно на внешней поверхности. Лимитирует перенос вещества из ядра потока к зерну. Энергия активации близка к нулю. Скорость сильно зависит от гидродинамики (скорости потока) и практически не зависит от температуры.
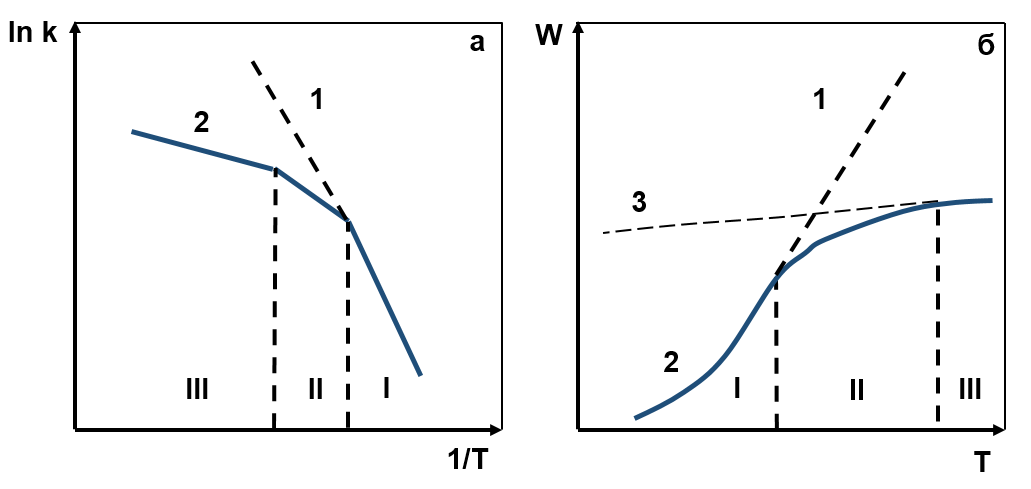
Зависимость конверсии (степени превращения) от температуры и кинетические области:
График (а): Зависимость логарифма константы скорости от обратной температуры. Линия 1 — идеальная кинетика (изломы отсутствуют); линия 2 — реальная зависимость с изломами, соответствующими смене лимитирующих стадий.
График (б): Зависимость скорости реакции W от температуры. Область I — при отсутствии диффузионного торможения; область II — при наличии диффузионного торможения; область III — при взаимодействии реагирующих веществ на наружной поверхности катализатора
График (а): Зависимость логарифма константы скорости от обратной температуры. Линия 1 — идеальная кинетика (изломы отсутствуют); линия 2 — реальная зависимость с изломами, соответствующими смене лимитирующих стадий.
График (б): Зависимость скорости реакции W от температуры. Область I — при отсутствии диффузионного торможения; область II — при наличии диффузионного торможения; область III — при взаимодействии реагирующих веществ на наружной поверхности катализатора
На рисунке справа представлена типичная S-зависимость конверсии СО от температуры на медно-марганцевых катализаторах.
Выделим две зоны протекания реакции : первая до пунктирной линии до 190⁰С, в которой ограничивающим фактором общей скорости протекания реакции служит кинетическое ограничение, то есть скорость химической реакции окисления СО на поверхности катализатора. При этом диффузия компонентов происходит быстрее и не является ограничением процесса.
Вторая зона после 190С, в которой лимитирующей стадией процесса окисления является внутренняя диффузия компонентов к поверхности катализатора. При этом скорость химической реакции окисления на поверхности катализатора становится существенно выше диффузии.
В момент пересечения пунктирной линии и графика происходит выравнивание скоростей химической реакции и диффузии реагентов СО и О2. В случае равенства скоростей каждой стадии процесса говорят о протекании каталитического превращения в смешанной области.
Повышение температуры приводит к увеличению диффузии компонентов к поверхности катализатора, а также диффузии конечных продуктов из зоны реакции.
В отличие от действия температуры катализаторы не влияют на скорость диффузии. Поэтому во многих случаях при значительном повышении скорости реакции суммарная скорость процесса остается низкой из-за медленного подвода компонентов в зону реакции.
Выделим две зоны протекания реакции : первая до пунктирной линии до 190⁰С, в которой ограничивающим фактором общей скорости протекания реакции служит кинетическое ограничение, то есть скорость химической реакции окисления СО на поверхности катализатора. При этом диффузия компонентов происходит быстрее и не является ограничением процесса.
Вторая зона после 190С, в которой лимитирующей стадией процесса окисления является внутренняя диффузия компонентов к поверхности катализатора. При этом скорость химической реакции окисления на поверхности катализатора становится существенно выше диффузии.
В момент пересечения пунктирной линии и графика происходит выравнивание скоростей химической реакции и диффузии реагентов СО и О2. В случае равенства скоростей каждой стадии процесса говорят о протекании каталитического превращения в смешанной области.
Повышение температуры приводит к увеличению диффузии компонентов к поверхности катализатора, а также диффузии конечных продуктов из зоны реакции.
В отличие от действия температуры катализаторы не влияют на скорость диффузии. Поэтому во многих случаях при значительном повышении скорости реакции суммарная скорость процесса остается низкой из-за медленного подвода компонентов в зону реакции.
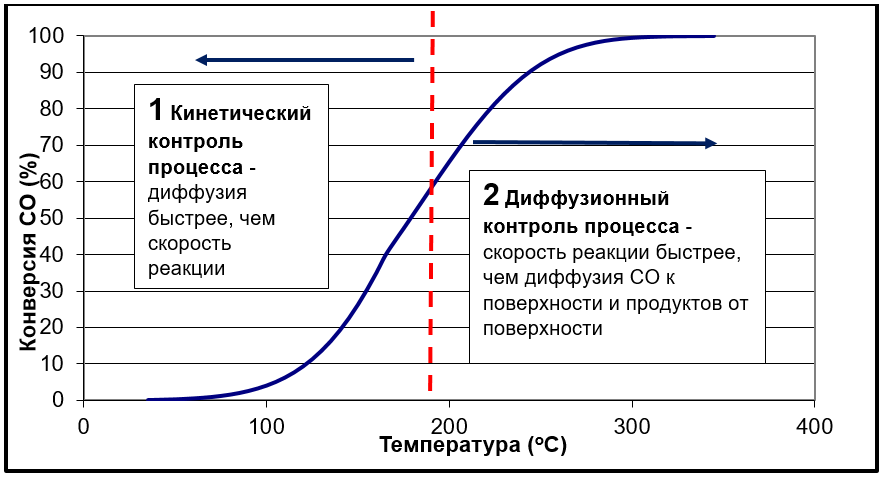
Типичная S-зависимость конверсии СО от температуры на медно-марганцевых катализаторах. На графике представлена S-образная кривая. На начальном участке (низкие T) — кинетический контроль процесса (медленный рост), затем крутой подъем (внутридиффузионная область) и выход на плато (внешнедиффузионная область, где конверсия перестает расти с температурой).
Практические аспекты и выводы
Для процессов каталитической очистки газов наиболее рациональной часто считается внешнедиффузионная область, так как она позволяет:
Современные исследования направлены на создание катализаторов, обеспечивающих протекание процесса в кинетической области при низких температурах (экономия энергии) либо во внешнедиффузионной области с минимальным гидравлическим сопротивлением и высокой турбулентностью потока. Процесс усовершенствования катализаторов окисления продолжается уже более 50 лет и остается актуальным направлением экологической инженерии.
- Использовать высокоактивные катализаторы.
- Добиться высокой степени очистки за доли секунды контакта.
- Снизить влияние колебаний расхода газа на степень очистки.
Современные исследования направлены на создание катализаторов, обеспечивающих протекание процесса в кинетической области при низких температурах (экономия энергии) либо во внешнедиффузионной области с минимальным гидравлическим сопротивлением и высокой турбулентностью потока. Процесс усовершенствования катализаторов окисления продолжается уже более 50 лет и остается актуальным направлением экологической инженерии.
Будем рады диалогу и сотрудничеству!
Оставьте контактные данные — мы свяжемся с вами в ближайшее время и предложим решение.
